
Manchmal haben scheinbar unbedeutende Details einen unglaublichen Einfluss auf das Gesamtbild. Dieses Prinzip gilt für viele Bereiche unseres Lebens: das mysteriöse Lächeln von Mona Lisa, das viele Theorien und Spekulationen hervorrief; eine Codezeile, die die Funktionalität des Programms vollständig ändern kann; die Reihenfolge der Anordnung der Atome, die die Eigenschaften einer Substanz verändert. Wir werden heute über Letzteres sprechen. Wissenschaftler der Universität Tsukuba (Japan) haben eine Theorie aufgestellt, nach der es möglich ist, eine neue Struktur aus Diamant zu erzeugen, die härter ist als das bekannte Mineral. Wissenschaftler nannten ihre Kreation "Pentadiamant". Was wird benötigt, um einen Pentadiamanten herzustellen, welche Eigenschaften kann er besitzen und wo kann solch eine ungewöhnliche Substanz verwendet werden? Antworten auf diese Fragen finden wir im Bericht der Wissenschaftler. Gehen.
Grundlagen der Forschung
Kohlenstoff ist ein allgegenwärtiges Element im Periodensystem und bildet die Grundlage für eine Vielzahl organischer und anorganischer Verbindungen. In der Natur kommt Kohlenstoff fast überall vor: Öl und Torf, Methan und Kohlendioxid, Muskeln und Knochen usw. usw. Kurz gesagt, Kohlenstoff wird aus einem bestimmten Grund als einer der Hauptbausteine des Lebens auf der Erde angesehen.
Bestimmte Substanzen oder chemische Elemente können unter verschiedenen Bedingungen in unterschiedlicher Form vorliegen. Dies nennt man Allotropie. Carbon ist der Rekordhalter in diesem Geschäft, da es mehr als 9 allotrope Modifikationen aufweist.
Die Gründe für das Vorhandensein einer so großen Anzahl von Kohlenstoff-Allotropen sind Orbitalhybridisierung, Randbedingungen und topologische Defekte. Drei Formen der Orbitalhybridisierung (sp, sp 2 und sp 3)) stellen Allotrope dar, die alle Dimensionen abdecken:
- eindimensionale Ketten für sp (Polyin);
- zweidimensionale Folie für sp 2 (Graphen);
- 3D-Netz für sp 3 (Diamant).
Darüber hinaus ermöglichen Randbedingungen und topologische Defekte, dass Kohlenstoff zusätzliche Allotrope mit einzigartigen Morphologien bildet: beispielsweise Fulleren- und Kohlenstoffnanoröhren, die ungewöhnliche elektronische und strukturelle Eigenschaften aufweisen.
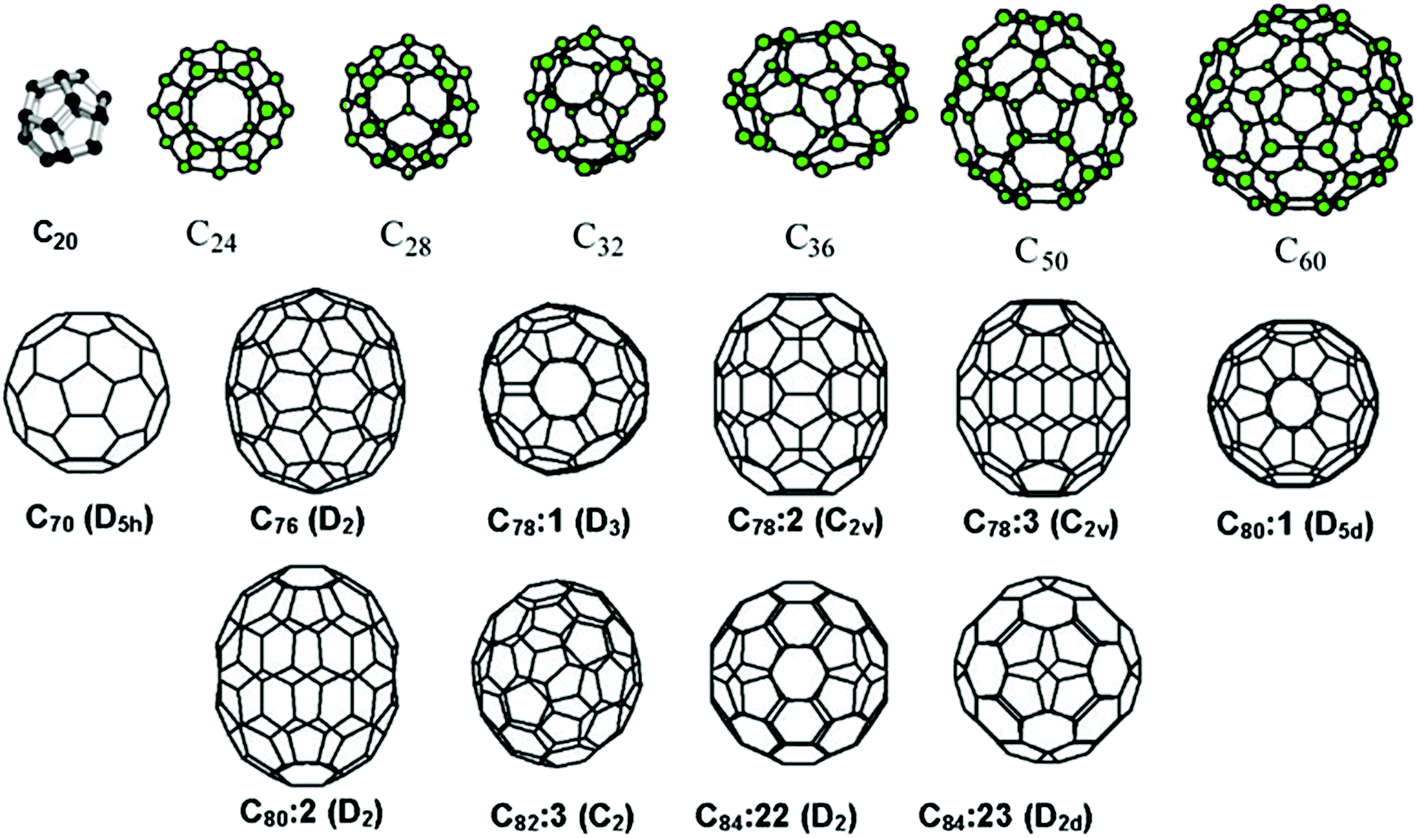
Eine Vielzahl von Fullerenen.
Kohlenstoff-Allotrope, die aus sp 2 - und sp 3 C-Atomen bestehen, ziehen die Aufmerksamkeit der Forscher aufgrund ihrer morphologischen Vielfalt auf sich, die auf die große Anzahl von Kombinationen von sp 2 - und sp 3 -Atomen innerhalb eines Systems zurückzuführen ist. Ein Beispiel hierfür sind Fullerene, die mit hohem Druck und hoher Temperatur behandelt wurden (z. B. C 60)), die aufgrund kovalenter Bindungen zwischen Fullerenen und Poren mit Nanogröße eine geringe Massendichte aufweisen können.
Darüber hinaus gibt es Studien, die das schnelle Löschen von amorphem Kohlenstoff beschreiben, was zur Bildung eines hybriden allotropen sp 2 -sp 3 -Q- Kohlenstoffs führt, dessen Magnetismus und Härte Diamant überlegen sind.
Kohlenstoff kann in den Händen von Wissenschaftlern grob als Plastilin bezeichnet werden, da man daraus viele Substanzen mit unterschiedlichen Eigenschaften und Funktionen herstellen kann, die Lust und Fantasie hervorrufen würden.
In dieser Arbeit präsentierten Wissenschaftler eine theoretische Studie eines dreidimensionalen Kohlenstoff-Allotrops, das aus den Atomen C sp 2 und sp 3 besteht(Pentadiamant). Es kann durch Copolymerisation von Kohlenwasserstoffmolekülen erhalten werden, die fünfeckige Ringe enthalten (Spiro [2.4] heptan-4.6-dien (C 7 H 8 ) und [5.5.5.5] -Phenestran-Tetrain).
Penta-Diamant besteht aus fünfeckigen Ringen mit der Raumgruppe Fm 3 m aufgrund der Copolymerisation dieser Molekülbestandteile. Berechnungen haben gezeigt, dass Pentadiamant einen hohen Volumenmodul * - 381 GPa aufweist, was ungefähr 80% des Diamanten entspricht. Dies legt nahe, dass Pentadiamant ein festes Kohlenstoff-Allotrop ist.
Darüber hinaus hat es ein negatives Poisson-Verhältnis * (-0,241), was zu einem extrem hohen Elastizitätsmodul * (1691 GPa) und Schermodul * führt (1113 GPa), was höher ist als der von Diamant oder anderen ultrastarken Kohlenstoffen.
Volumenelastizitätsmodul * - ein Merkmal der Fähigkeit eines Stoffes, einer Rundumkompression zu widerstehen.
Poisson-Verhältnis * - das Verhältnis der relativen seitlichen Kompression zur relativen Längsspannung.
Elastizitätsmodul * (Elastizitätsmodul) - eine Bewertung der Fähigkeit eines Materials, Zug und Druck unter elastischer Verformung zu widerstehen.
Schermodul * - eine Bewertung der Fähigkeit des Materials, einer Scherverformung zu widerstehen.Penta-Diamant ist ein Halbleiter mit einer indirekten Bandlücke * von 2,25 eV, von der eine hohe Lochbeweglichkeit * erwartet wird .
* — , .
* — .
Alle Berechnungen wurden auf Basis der im STATE-Softwarepaket ( STF-ElectronMo ) implementierten Dichtefunktionaltheorie durchgeführt .
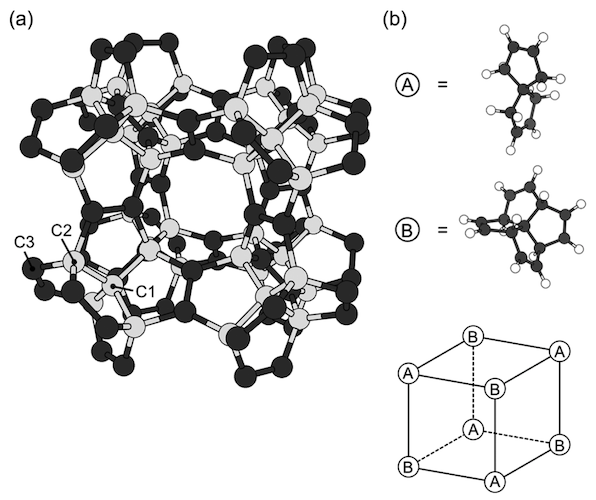
Bild 1
Die obigen Diagramme zeigen die optimierte Geometrie eines Fünfecks mit einem Gitterparameter von 9,195 Å und einer Raumgruppe Fm 3 m. Das kovalente Netzwerk besteht ausschließlich aus Pentagonen, bei denen drei der fünf Kanten durch benachbarte Pentagone ( 1a ) aufgrund der Copolymerisation von C 7 H 8 und [5.5.5.5] -Phenestran-Tetrain getrennt sind, die sich abwechselnd an den Eckpunkten des kubischen Gitters befinden ( 1b ).
Entsprechend diesen Molekülbestandteilen und ihrer Anordnung enthält die Elementarzelle eines Petadiamanten 22 Kohlenstoffatome: 10 sind sp3 und 12 - durch sp 2 Atome . Zusätzlich reduzieren die Symmetrieoperatoren, die zur Gruppe Fm 3m gehören, die Anzahl unabhängiger Atomregionen auf drei.
Da das Netzwerk aus sp 2 (dreifach koordiniert) und sp 3 (vierfach koordiniert) Kohlenstoffatomen besteht , werden kovalente Bindungen in zwei Gruppen eingeteilt. Die berechneten Bindungslängen in Bezug auf sp 3 -Atome betragen 1,563 Å für C1-C1-Bindungen und 1,520 Å für C2-C3. Die Bindungslänge (C3-C3) für sp 2 -Atome beträgt jedoch 1,349 Å, was das Vorhandensein einer Doppelbindung in sp 2 -Atomen bestätigt .
Wie in 1a gezeigtPentadiamant hat große kubische "Poren" mit 3,664 Å Kanten, die von einem fünfeckigen kovalenten Netzwerk umgeben sind. Folglich hat es eine geringe Massendichte mit einer Dichte von 2,26 g / cm 3 wie Graphit, jedoch 36% weniger als Diamant.
Die relative Gesamtenergie eines Pentadiamanten beträgt 275 meV / Atom, was einem klassischen Diamanten entspricht. Die Gesamtenergie ist jedoch höher als die von Diamant, Graphit und anderen harten Kohlenstoffmaterialien, wenn auch niedriger als die von C60, das als metastabiles nulldimensionales Kohlenstoff-Allotrop bekannt ist. Die moderate Gesamtenergie erklärt sich aus der strukturellen Verzerrung der Bindungswinkel für sp 2 - und sp 3 -Atome .
In Bezug auf sp 3 -Atome : trotz der Tatsache, dass das C1-Atom eine nahezu perfekte sp hat3 Hybridisierung mit einem Bindungswinkel θ212 = 109,4 °, hat das C2-Atom Bindungswinkel θ212 = 115,9 ° und θ323 = 101,9 °, die breiter und schmaler sind als die entsprechenden Bindungswinkel von idealem sp 3 . In Bezug auf sp 2 -Atome : Aufgrund des fünfeckigen Netzwerks beträgt der Bindungswinkel in Bezug auf C3 θ232 = 133,4 ° und θ233 = 113,3 °, was ebenfalls größer und kleiner als die entsprechenden Bindungswinkel für ideales sp 2 ist .
Mäßige Energie erhöht auch die Bildungsenergie (ΔE) von Pentadiamant bei direkter Copolymerisation von C 7 H 8 und [5.5.5.5] -Phenestran-Tetrain:
Spironadien + Fenestratetraen = Pentadiamant + 12H 2 + ΔEDie berechnete Bildungsenergie beträgt 0,31 eV / Atom, was den Energieverbrauch für die Bildung eines kovalenten Netzwerks von sp 2 - und sp 3 -Kohlenstoffatomen mit verzerrten Bindungswinkeln widerspiegelt.
Daher wird erwartet, dass Pentadiamant unter Verwendung der Ullmann-Reaktion für Bromospiro [4.4] nona-2.7-dien und Brom [5.5.5.5] -phenestratetraen anstelle ihrer primären Form synthetisiert wird.
Als nächstes untersuchten wir die thermische Stabilität von Pentadiamanten durch Simulation der Molekulardynamik bei einer Temperatur von 4000 K. Um zu verstehen, welche Strukturänderungen auftreten können, wurden molekulardynamische Berechnungen mit einer konstanten Temperatur für eine expandierte Atomzelle (88 Kohlenstoffatome) für 12 ps (Pikosekunden, 1 ps =) durchgeführt 10-12 s) und für eine vereinfachte (1x1x1) für 146 ps.
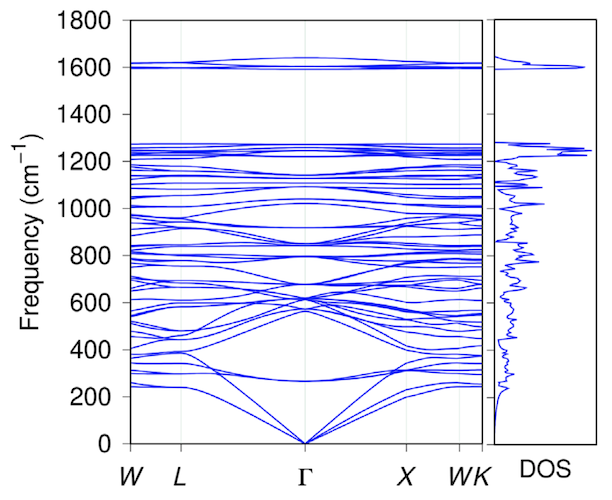
Bild 2
Gemäß den Simulationsergebnissen nach 14 ps bei 4000 K behält der Pentadiamant seine ursprüngliche Topologie sowohl in der komplexen als auch in der vereinfachten Atomzelle vollständig bei (Grafik oben).
Folglich ist Pentadiamant thermisch und energetisch stabil, wenn es unter Verwendung der in dieser Arbeit vorgeschlagenen geeigneten Schemata synthetisiert wird.
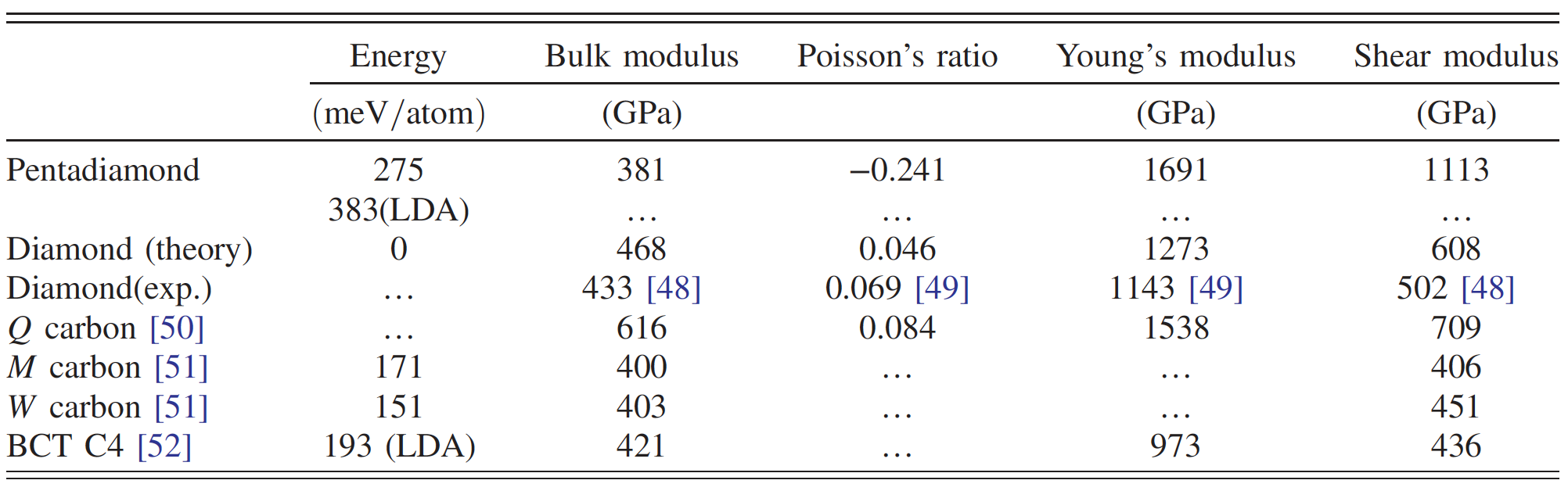
Vergleich der Eigenschaften von Penta-Diamant und anderen Kohlenstoff-Allotropen.
Die mechanischen Eigenschaften von Pentadiamanten wurden mit Hilfe der elastischen Konstanten cij untersucht, die durch Auswertung der endlichen Differenz der Gesamtenergie in Bezug auf Verformungen bestimmt werden. Die berechneten Werte der elastischen Konstanten waren: 1715,3 GPa für s 11 (= s 22 = s 33 ); −283,5 GPa für s12 (= s 13 = s 23 ) und 1187,5 GPa für s 44 (= s 55 = s 66 ).
Es ist auch zu beachten, dass diese Indikatoren das Born-Stabilitätskriterium (mit 11 - mit 12 > 0, mit 11 + 2c 12 > 0 und mit 44 > 0) vollständig erfüllen , was zusätzlich die Stabilität von Pentadiamanten anzeigt.
Bei kubischer Symmetrie wird der Volumenelastizitätsmodul nach folgender Formel berechnet: B = (s 11 + 2s 12) / 3. Infolgedessen war B gleich 381 GPa, was mehr als 80% der entsprechenden Zahl für Diamant entspricht. Dies legt nahe, dass Pentadiamant ein potenzieller Kandidat für Allotrope aus festem Kohlenstoff ist, obwohl seine Dichte ziemlich niedrig ist (wie die von Graphit).
Zur weiteren Untersuchung der mechanischen Eigenschaften wurde der Elastizitätsmodul von Penta-Diamant nach folgender Formel berechnet:
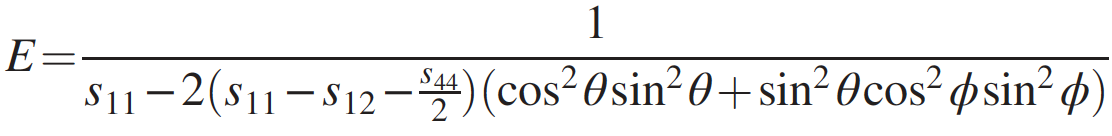
wobei θ und ϕ die Euler-Winkel * sind , ist s ij die durch cij bestimmte elastische Übereinstimmung mit den Beziehungen zwischen s 11 = [c 11 + c 12 ] / [(c 11) - c 12 ) (c 11 + 2c 12 )], s 12 = [-c 12 ] / [(c 11)- c 12 ) (c 11 + 2c 12 )] und s 44 = 1 / c 44 .
Eulerwinkel * - Winkel, die die Drehung eines absolut starren Körpers im dreidimensionalen Raum beschreiben.
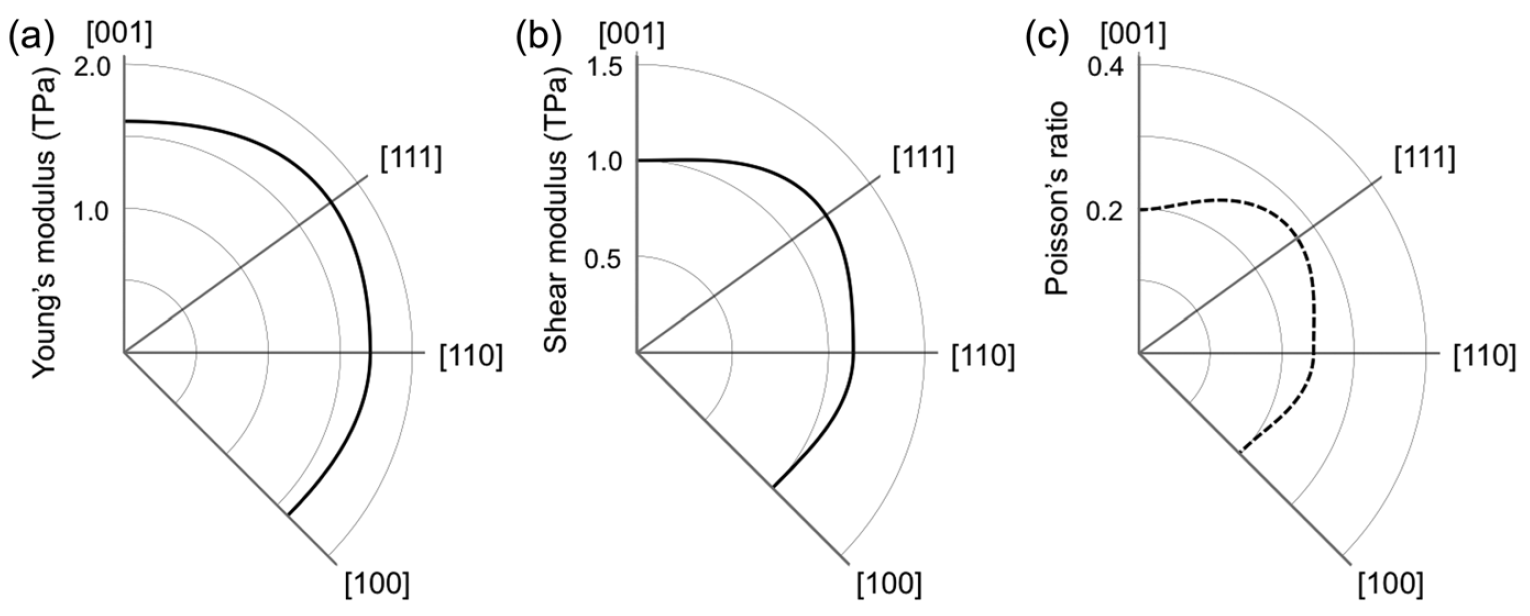
Bild Nr. 3
Der Elastizitätsmodul von Penta-Diamant ist extrem hoch und überschreitet 1,5 TPa für alle Richtungen ( 3a ). Wenn man den Elastizitätsmodul und den Volumenelastizitätsmodul kennt, kann man den Schermodul ( 3b ) berechnen , der sich auch für alle Richtungen als ziemlich hoch (1 TPa) herausstellte.
Folglich kann Pentadiamant eine extreme Steifheit in Bezug auf anisotrope strukturelle Verformungen aufweisen. Besondere Aufmerksamkeit erfordert auch die Tatsache, dass der Elastizitätsmodul und der Schermodul höher sind als bei anderen harten und superharten Kohlenstoff-Allotropen (Tabelle oben).
Solche hohen Werte der oben beschriebenen Module zeigen an, dass der Pentadiamant ein negatives Poisson-Verhältnis haben sollte. Diese Aussage wurde durch Berechnungen bestätigt, die das Poisson-Verhältnis im Bereich von -0,20 bis -0,28 in Abhängigkeit von den Richtungen des Gitters ( 3c ) zeigten . Solche einzigartigen Indikatoren führen dazu, dass die Schallgeschwindigkeit in Pentadiamanten ebenfalls recht hoch ist (28700 m / s gegenüber 12000-18350 m / s bei gewöhnlichen Diamanten).
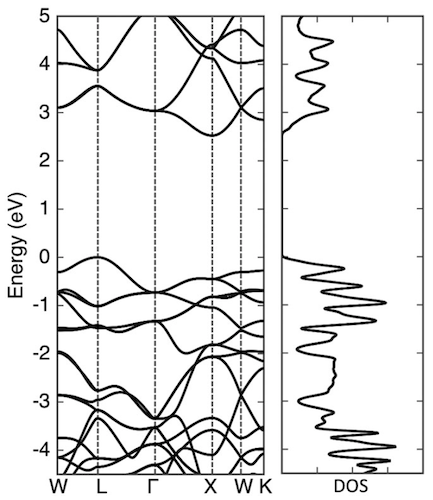
Bild Nr. 4
Die obige Grafik zeigt die elektronische Struktur und Dichte der Zustände von Pentadiamant, einem Halbleiter mit einer indirekten Bandlücke von 2,52 eV. Die Valenz- und Leitungsbänder befinden sich an den Punkten L bzw. X. Der höchste Zweig des Valenzbandes und der niedrigste Zweig des Leitungsbandes weisen eine signifikante Dispersion auf (1 eV oder mehr).
Daher wird erwartet, dass Pentadiamant an den Rändern der Bänder kleine effektive Massen aufweist: Die berechneten Elektronenmassen am Punkt X betragen 0,98 und 0,67 (weniger als die von Diamant) entlang der Richtungen zu den Punkten Γ bzw. W. In Bezug auf den Rand des Valenzbandes ist die Situation jedoch umgekehrt: Die berechneten Lochmassen am Punkt L betragen 1,59 und 0,76 (größer als die von Diamant) entlang der Richtungen zu den Punkten W bzw. Γ.
Die moderate Trägermasse und die hohe Zustandsdichte an den Bandkanten legen nahe, dass Pentadiamant sowohl für ein Elektron als auch für ein Loch eine moderate Trägermobilität aufweisen kann. Die Dispersionsrelation sowie die Zustandsdichte zeigen, dass Pentadiamant wie ein Diamant eine dreidimensionale volumetrische elektronische Struktur aufweist, die sein dreidimensionales kovalentes Netzwerk mit hoher Symmetrie widerspiegelt.
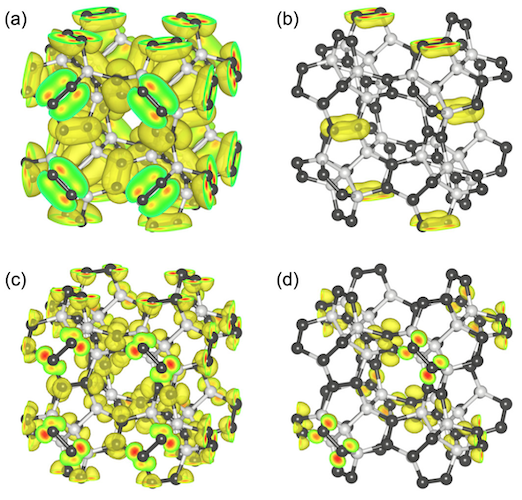
Bild №5
Zum besseren Verständnis der elektronischen Struktur von Pentadiamanten führten die Wissenschaftler eine Untersuchung der Wellenfunktion des höchsten und des niedrigsten Zweigs von Pentadiamanten an bestimmten Symmetriepunkten durch.
Die Wellenfunktionen des höheren Zweigs des Valenzbandes an den Punkten L und Γ sind aufgrund ihres sp 2 über die C3-Atome verteilt, die den Charakter einer π-Bindung haben-Hybridisierung. Die Wellenfunktion des unteren Zweigs des Leitungsbandes an den Punkten Γ und X ist ebenfalls über die C3-Atome mit einer antibindenden π-Natur verteilt. Wissenschaftler stellen fest, dass sowohl der Valenzzustand als auch der Leitungszustand kein reiner π-Zustand sind, sondern hybridisierte Zustände, die eine kleine Menge der σ-Komponente enthalten. Dies bedeutet, dass die elektronischen Zustände in der Nähe und um die Bandkanten als π-elektronische Zustände von sp 2 C- Dimeren betrachtet werden , die ungefähr 2,6 Å von ihren acht benachbarten Regionen entfernt sind.
Um die Nuancen der Studie genauer kennenzulernen, empfehle ich Ihnen, den Bericht von Wissenschaftlern zu lesen .
Epilog
In dieser Studie haben Wissenschaftler die Theorie weiterentwickelt, dass es möglich ist, eine Kohlenstoffstruktur mit besseren Eigenschaften als Diamant zu erzeugen. Die während der Studie durchgeführten Berechnungen bestätigten diese Vermutung.
Durch Copolymerisation von Spiro [2.4] heptan-4.6-dien (C 7 H 8 ) und [5.5.5.5] -Phenestrantetrain mit Fm ¯ 3m-Symmetrie kann ein dreidimensionales kovalentes fünfeckiges Netzwerk von sp 2 - und sp 3 -Kohlenstoffatomen synthetisiert werden . Wissenschaftler nannten ihre Kreation einen Pentadiamanten.
Die meisten mechanischen Eigenschaften von Pentadiamanten sind denen von uns bekannten herkömmlichen Diamanten oder anderen Allotropen aus hartem Kohlenstoff überlegen. Seltsamerweise ist Pentadiamant härter als Diamant, aber seine Dichte ähnelt der von Graphit.
Wissenschaftler wollen in Zukunft Theorie in die Praxis umsetzen. Aber selbst jetzt zeigt ihre Arbeit deutlich, dass die Möglichkeiten der modernen Wissenschaft wirklich endlos sind, wenn Sie natürlich auf Details achten, sich an alle Nuancen der Naturgesetze erinnern und keine Angst vor Experimenten haben.
Freitag off-top:
BBC , . ( , )
BBC , . ( , )
Off-Top 2.0:
, , ? , , .. - …
, , ? , , .. - …
Vielen Dank für Ihre Aufmerksamkeit, bleiben Sie neugierig und haben Sie ein tolles Wochenende Jungs! :) :)
Ein bisschen Werbung
Vielen Dank für Ihren Aufenthalt bei uns. Gefällt dir unser Artikel? Möchten Sie weitere interessante Inhalte sehen? Unterstützen Sie uns, indem Sie eine Bestellung aufgeben oder Freunden Cloud-VPS für Entwickler ab 4,99 US-Dollar empfehlen , ein einzigartiges Analogon von Einstiegsservern, das wir für Sie erfunden haben: Die ganze Wahrheit über VPS (KVM) E5-2697 v3 (6 Kerne) 10 GB DDR4 480 GB SSD 1 Gbit / s ab 19 $ oder wie teilt man den Server? (Optionen sind mit RAID1 und RAID10, bis zu 24 Kernen und bis zu 40 GB DDR4 verfügbar).
Dell R730xd ist im Equinix Tier IV-Rechenzentrum in Amsterdam 2x billiger? Nur wir haben 2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2,6 GHz 14C 64 GB DDR4 4 x 960 GB SSD 1 Gbit / s 100 TV von 199 US-Dollar in den Niederlanden!Dell R420 - 2x E5-2430 2,2 GHz 6C 128 GB DDR3 2x960 GB SSD 1 Gbit / s 100 TB - ab 99 US-Dollar! Lesen Sie mehr über den Aufbau eines Infrastrukturgebäudes. Klasse mit Dell R730xd E5-2650 v4 Servern für 9.000 Euro pro Penny?