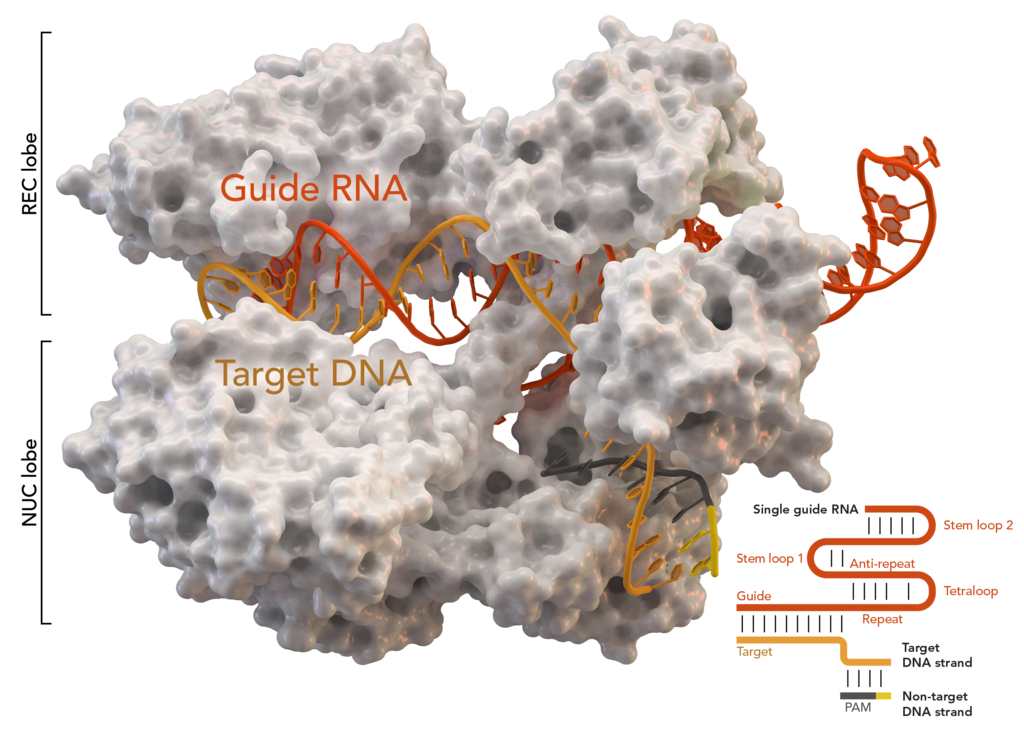
Kristallstruktur von S. aureus Cas9 in einem Komplex mit crRNA und seiner Ziel-DNA
In früheren Beiträgen haben Sie darum gebeten, mehr über CRISPR / Cas9 und Ansätze zur Bearbeitung des Genoms zu erfahren. Ich habe einfach kein so umfangreiches Material in den letzten Beitrag aufgenommen. Und dazu werde ich zum Beispiel nicht die TALEN-Methode einbeziehen, die möglicherweise genauer sein kann und ihre Vorteile hat. Aber Liebling, ja.
Lassen Sie uns versuchen, die bereits gut beschriebene Methode der genetischen Veränderung mit CRISPR-Cas9 durchzugehen und die Perspektiven, die sich daraus für uns ergeben, etwas genauer zu betrachten. Ich war sehr interessiert an der Richtung der xenogenen Transplantation von Schweinen auf Menschen. Die erste "Vorkorrektur" -Methode zeigte, dass eine solche Schweinetransplantation vom inneren Körper abgetötet wird ein paar Minuten . Aber die Methode wurde überhaupt nicht verworfen. Dies ist jedoch eine vielversprechende Möglichkeit, nicht zu warten, bis ein anderer potenzieller Organspender stirbt, sondern sie im Voraus zu züchten. Dann stellte sich heraus, dass Schweine auch eine Packung spezifischer Retroviren tragen, die in ihr Genom eingebaut sind und eine Epidemie einer neuen Xenozoonose verursachen können. Und auch Viren müssen vor der Transplantation irgendwie herausgesucht werden. Und irgendwo hier erscheinen Menschen in weißen Kitteln auf der Bühne und tun etwas Unverständliches in ihren Labors ...
Das bakterielle Antivirus, das alles auf den Kopf gestellt hat
1987 wurde CRISPR von japanischen Wissenschaftlern unter der Leitung von Yoshizumi Ishino entdeckt. Zu dieser Zeit machten sie auf die ungewöhnlichen Wiederholungen im E. coli-Genom aufmerksam, legten jedoch keinen besonderen Wert darauf. Und erst als ähnliche Wiederholungen in Archaeen gefunden wurden, die genetisch sehr weit von E. coli entfernt sind, begannen sie, nach ähnlichen Strukturen in anderen Prokaryoten zu suchen. Diese Schnipsel werden als CRISPR - Clustered Regular Interspaced Short Palindromic Repeats bezeichnet. Wenig später wurden auch spezielle CRISPR-assoziierte Proteine, Cas ( CRISPR als assoziiertes Protein), entdeckt. Gut entdeckt und entdeckt, wie es scheint. Aber sie waren der Beginn einer neuen biotechnologischen Revolution.
Jetzt werde ich versuchen, Ihnen zu sagen, wie es funktioniert und warum Bakterien es brauchen. Die Bakterien würden gerne überleben. Aber sie parasitieren gerne Viren. Wenn dich jemand isst, ist das unangenehm und du musst etwas tun. Infolgedessen war die Antwort ein komplexer, aber äußerst interessanter Mechanismus. Das Bakterium speichert die Signaturen aller Bösewichte, die versuchen, es zu infizieren, in einem Stück seines Genoms. Dies sind die gleichen sich wiederholenden palindromischen Regionen - CRISPR. Sie arbeiten mit Proteinen aus der Cas-Gruppe zusammen. Wir interessieren uns für den Schlüssel Cas9. Wie sieht es live aus, wenn es ein wenig vereinfacht wird?
Wenn dieses System nicht funktioniert, kann die Bakterienzelle das vom Bakteriophagen sorgfältig eingeführte virale Genom nicht von seinem eigenen unterscheiden. Und das nicht sehr clevere System der Proteinsynthese wird sofort auf die Freisetzung neuer Generationen von Phagen ausgerichtet. Die Zelle stirbt.
Wenn CRISPR / Cas9 ausgelöst wird, ist der Prozess anders. Das Bakterium verwendet die in CRISPR aufgezeichneten Daten, um Kontroll-RNA zu erzeugen. Der Proteinkomplex beginnt, die DNA zum Testen vor dem "Start" abzuwickeln. Falls die Sequenz mit den in CRISPR aufgezeichneten Virensignaturen übereinstimmt, löst Cas9 den Alarm aus und schneidet das erkannte feindliche Fragment sofort ab. Das heißt, selbst wenn ein Virus auf der „Firmware“ -Ebene in das Bakteriengenom eingebettet ist, wird es von dort abgeschnitten, sobald das eingebaute Antivirus es erkennt.
Nobelpreis
Emmanuelle Charpentier und Jennifer Doudna erhielten 2020 den Nobelpreis für Chemie für die Entwicklung neuer Technologien, mit denen CRISPR-Cas9 die Bearbeitung des Genoms durchführen kann. Diese Technologie ermöglichte es, die damals genaueren, aber komplexeren und teureren Methoden von Zinkfingern und TALEN-Nukleasen zu ersetzen. Frühere Methoden erforderten die Entwicklung, Expression und Validierung eines völlig neuen Polypeptidpaars für jeden neuen Zielort. Und CRISPR-Cas9 gab ein Standardwerkzeug, bei Verwendung in der Minimalversion reicht es aus, die erforderliche Kontrollsequenz zu erhalten, nach der Cas9 den für die Dissektion erforderlichen Bereich findet.
Okay, wir haben DNA von einem Menschen, einer Hefe oder einer Testratte geschnitten. Das ist cool, aber jetzt haben wir zwei zerbrochene Teile und eine zerstörte Kette. Es gibt verschiedene Möglichkeiten zum Zurücknähen.

Sie können versuchen, die geschnittenen Teile mit der nicht homologen Endverbindungsmethode abzugleichen. Er ist auf der rechten Seite. Um es einfach auszudrücken: In dieser Version versuchen wir einfach, die Doppelunterbrechung direkt anzudocken und zu einem einzigen Ganzen zu verschweißen. Dieser Mechanismus ist ziemlich unwirksam, da beim "Anpassen" einzelne Endabschnitte herausfallen können. Infolgedessen gehen häufig kleine Fragmente in der Bruchzone verloren oder es treten im Gegenteil kurze Einsätze auf. Dieser Ansatz schaltet das Gen normalerweise irreversibel aus und macht es defekt.
Die zweite Option ist interessanter. Er ist in der Abbildung rechts. Die Reparatur durch homologe Rekombination impliziert das Ersetzen einer gelöschten Sequenz durch eine neue Sequenz, die zu einer vom Forscher selbst erstellten Reparaturvorlage komplementär ist. Infolgedessen ist es möglich, das Gen nicht nur irgendwie auszuschalten, sondern die mutierte Sequenz durch die normale zu ersetzen.
Das Hauptproblem bei der Methode ist, dass sie probabilistisch ist. Ja, in einem großen Prozentsatz der Fälle funktioniert es genau so, wie es sollte. Aber in vielen Zellen wird es entweder nicht den gewünschten Effekt erzielen oder etwas zur Hölle brechen. Und es ist gut, wenn nur einzelne Zellen daran sterben und beispielsweise nicht zu Tumorzellen werden. Daher müssen alle derartigen Änderungen gründlich getestet werden. Zum Glück relativ frische Ansätze Um die Spezifität durch Erstellen eines benutzerdefinierten Cas9 zu verbessern, kann die Anzahl fehlerhafter Schnitte auf nahezu Null reduziert werden.
Xenotransplantate
Wie ich bereits sagte, stoppt der massive Einsatz dieser Techniken die Spezifität. Wenn unser wunderbares Molekül einfach 20% der Zellen verfehlt, ist das keine große Sache. Dies bedeutet, dass 80% der menschlichen Zellen mit einer angeborenen Mutation fixiert sind und bereits beginnen, das richtige Enzym zu produzieren, sich angemessen zu teilen oder etwas anderes richtig zu machen. In der Regel ist dies mehr als genug, um klinisch gesund zu werden.
In diesem Abschnitt möchte ich ein wenig darüber sprechen, wie die Bearbeitung des Genoms möglicherweise das Problem der Organspende lösen kann. Ich muss sagen, dass der Mangel an Organen für die Transplantation sehr traurig aussieht. Riesige Wartezeiten und viele ethische Fragen.
Die Anzahl der in Russland durchgeführten Organtransplantationen ist hunderte Male niedrigerBedürfnisse. Wenn dieselbe Niere von einem geeigneten Verwandten transplantiert werden kann, bedeutet eine Herztransplantation bereits den Tod des Spenders. Einer der Schlüsselbereiche bei der Suche nach einer unbegrenzten Organquelle ist die Xenotransplantation. Dies ist eine Option zum Transplantieren von Geweben und Organen zwischen verschiedenen Arten. Seltsamerweise ist ein Schwein in Struktur und Größe für den Menschen am besten geeignet . Primaten sind zwar genetisch näher, aber im Allgemeinen viel kleiner und in der Zucht sehr teuer. Leider zeigten frühe Experimente mit Schweineorgantransplantationen, dass sie innerhalb weniger Minuten nach dem Anschluss an den Blutkreislauf mit einer hyperakuten Reaktion abzustoßen beginnen.
Wie man ein Schwein modifiziert

Damit das Transplantat nicht abgestoßen wird, müssen zumindest die Zielgene, die für die Synthese der fremdesten Proteine für uns verantwortlich sind, ausgeschaltet werden. Das erste derartige Protein ist das Enzym Alpha-1,3-Galactose, das bei allen Primaten im Verlauf der Evolution irreversibel gebrochen wird. Er ist es, der innerhalb weniger Minuten den Beginn der Ablehnung verursacht . Durch die Genkorrektur konnte eine Schweinerasse erzeugt werdenmit einem ausgeschalteten Gen, das für die Synthese des Enzyms Schwein GTKO verantwortlich ist. Obwohl dies den Ablehnungsprozess erheblich verlangsamte, wurde es nicht vollständig gestoppt. Es stellte sich heraus, dass N-Glycolylneuraminsäure und β1,4-N-Acetylgalactosaminyltransferase, die in Primaten fehlen, ebenfalls problematisch sind. Diese Gene wurden ebenfalls ausgeschaltet und die Schweine GGTA1 / CMAH / β4GALNT2 KO wurden erhalten, wobei alle drei Gene gleichzeitig ausgeschaltet waren. Vermutlich kann dies die Abstoßungsreaktion praktisch neutralisieren . Wenn sich theoretisch herausstellt, dass auch Schweinezellen gezwungen werden, das Oberflächenglykoprotein CD47 einer Person zu synthetisieren, ist die Kompatibilität ziemlich gut .
2018 gab es eine vielversprechende Veröffentlichungzur Herztransplantation von GVO-Schweinen zu Pavianen. Von den 5 Pavianen hatte nur einer Probleme, das Lungenödem begann aus chirurgischen Gründen und musste vorab aus dem Experiment genommen werden. Der Rest überlebte bis zum Ende ihrer Versuchsperiode bei guter Gesundheit. Zwei bis drei Monate und zwei bis sechs Monate. Es gab einige Probleme aufgrund des Wachstums des Organs, da das Herz eines Schweins größer ist als das eines Pavians, aber für eine Person wird dies kein Problem sein.
Steht ein neues HIV vor uns?

Phylogenetischer Baum von HIV und verwandten Viren bei Schimpansen
Es scheint, dass eine glänzende Zukunft auf uns wartet, in der eine separate Herde spezieller Laborschweine für die Produktion von Spenderorganen weiden wird. Aber auch hier treten viele ethische Probleme auf. Ich vermute, dass eine solche Methode für Vertreter mehrerer Religionen nicht akzeptabel sein wird, was sie automatisch für einen großen Teil der Weltbevölkerung unzugänglich macht.
Schweine haben auch Retroviren. Dazu gehören beispielsweise ein so wunderbares Lentivirus wie das humane Immundefizienzvirus und verwandte Primatenviren. Es wird angenommen, dass es das Primatenvirus war, das in den 70er Jahren des letzten Jahrhunderts die massive HIV-Epidemie auslöste. Und jetzt weiß ein Mensch nicht, was er mit ihm anfangen soll. Schweine sind Träger von PERVs - endogenen Schweine-Retroviren. Und Sie können diese Viren nicht durch sorgfältige Züchtung und antiepidemische Maßnahmen loswerden, da die Viren bereits fest im Genom ihrer Zellen verankert sind. Forschung wurde durchgeführt das sollte eine mögliche Lösung geben. Zunächst nahmen sie Schweinezellen und züchteten sie in derselben Kultur wie embryonale Zellen aus einer menschlichen Niere. Das Ärgerlichste ist, dass sie menschliche Zellen identifizieren konnten, die mit Schweine-Retroviren infiziert waren, was möglicherweise auf eine solche Möglichkeit einer Transplantation hinweist. Als Lösung schlugen sie die Vorverarbeitung von Zellen mit CRISPR-Cas9 und die vollständige Entfernung aller Virusfragmente aus der Kultur von Schweine-Nierenepithelzellen vor.
Biotech und Risiken
Wohin dies alles führen wird, ist schwer vorherzusagen. Leider ist das Risiko, eine exotische Virusmutante aus einer solchen Transplantation zu erhalten, weit von Null entfernt. Und es besteht die Möglichkeit, dass sich eine solche Infektion auch leise und unmerklich ausbreitet, bevor sie offensichtlich wird, wie es zu seiner Zeit mit HIV geschehen ist. Und doch bin ich eher optimistisch. Wir werden im Forschungsprozess unweigerlich auf viel Rechen setzen, aber jetzt haben wir die Werkzeuge, um zuvor tödliche Krankheiten zu behandeln und das Leben der Menschen zu verlängern.
