
Ich frage mich, wie unsere Forschung enden wird.
Es scheint, dass das vergangene Thema über GVO-Lachs für Habrachiter recht gut angekommen ist. Während wir Material zur Pflanzenmodifikation vorbereiten, schlage ich vor, ein ebenso interessantes Thema zu betrachten - die genetische Modifikation des Homo Sapiens. Dies ist ein sehr kontroverses und ganzheitliches Thema, das man nicht ignorieren kann.
Ich werde sofort einige Thesen geben, die kontrovers erscheinen mögen, aber in der wissenschaftlichen Gemeinschaft irgendwie gelöst werden müssen:
- Wir degenerieren. Jedes Jahr überleben schwächere Individuen, gebären Kinder und belasten den Genpool. Es muss behoben werden.
- Einfache Verbote helfen nicht. Wenn Experimente in Europa verboten sind, wird China sie beispielsweise durchführen.
- Wir werden nicht aufhören, genetische Krankheiten zu behandeln. Früher oder später wird sich das Militär mit seinen Supersoldaten und denen zusammenschließen, die stärkere und klügere Kinder mit blauen Augen wollen.
Ich werde versuchen, einen Überblick über die bestehenden Techniken der Intervention in den Genotyp von Menschen zu geben, und gleichzeitig werden wir analysieren, womit es uns bedroht.
Was ist Gentherapie?
Definieren wir zunächst die Terminologie. Gentherapie ist eine Intervention in das menschliche Genom mit dem Ziel, bestimmte Krankheiten zu behandeln. Darüber hinaus erfolgt die Intervention nur in somatischen Zellen. Dies sind die Zellen, die sich nicht vermehren. Wir müssen eindeutig keine Mutationen und Fehlerbehebungen in neuen Generationen beheben. Zumindest für den Moment.
Echte Tierversuche begannen um die 1980er Jahre, aber dann waren es nur schüchterne Schritte. Wir hatten keine Schönheit wie DNA-Drucker, die Vektoren für Eukaryoten exprimierten.
Wo können wir wirklich eingreifen?
Plasmide
Zunächst können Sie den Zellkern verlassen, der die grundlegenden genetischen Informationen enthält. Sie können Plasmide verwenden.

1) Chromosomale DNA von Bakterien 2) Plasmide
Plasmide sind fast ausschließlich bakteriell. Manchmal in primitiven Pilzen und einigen Pflanzen gefunden. Tatsächlich ist dies DNA, die jedoch zu einem Ring gefaltet ist und separat im Zytoplasma schwimmt. Das heißt, ein solcher separater Mechanismus zum Speichern von genetischem Material. Für Bakterien sind sie sehr wichtig für die Übertragung positiver Mutationen, um beispielsweise Nachbarn über Antibiotika-Schutzoptionen zu informieren. Der Trick von Plasmiden beim Menschen besteht darin, dass sie nach einiger Zeit nach dem Einbringen in die Zelle von selbst auseinanderfallen. Und sie beeinflussen auch nicht den genetischen Hauptapparat der Zelle. Das heißt, die Hauptfirmware ist nicht betroffen.
Kernel patchen
Als nächstes haben wir die Möglichkeit, das Code-Snippet direkt im Kernel zu bearbeiten. Dies ist ein invasiveres Verfahren und birgt bereits das Risiko, dass ein DNA-Stück ungenau eingeführt oder ausgeschnitten wird. Dies ist jedoch praktisch die einzige Möglichkeit, einen schwerwiegenden genetischen Defekt radikal zu beheben, da sich somatische Zellen teilen und die gepatchte Version der DNA an ihre Nachkommen übertragen.
Mitochondrien
Mitochondrien sind wie Kernreaktoren in einer Zelle. Sie verbrauchen Fettsäuren und Glukose und prägen am Ausgang Makroerge - Substanzen mit hoher Bindungsenergie. Zum Beispiel ATP. Es ist ein universeller "Brennstoff" für alle aktiven Reaktionen, beispielsweise für den Betrieb von osmotischen Membranpumpen gegen einen Konzentrationsgradienten.
Sie haben eine Besonderheit - ihren eigenen genetischen Apparat. Tatsächlich sehen sie aus genau diesem Grund wie halbautonome Symbionten aus. Ihr genetischer Apparat ist sinnvoll, um mit angeborenen Mutationen in der mitochondrialen DNA zu regieren. In der Regel handelt es sich auch um sehr schwere angeborene Syndrome.
Der virale Vektor ist wie eine Spritze
Der erste wichtige Punkt ist die Entwicklung von Abgabewerkzeugen - viralen Vektoren. Der erste derartige Virus für Säugetiere wurde entwickelt im Jahr 1984. Ein murines Retrovirus wurde als molekulare Spritze verwendet. Er an sich war ein sehr unangenehmes Werkzeug, da es mit hoher Wahrscheinlichkeit onkologische Erkrankungen hervorrief. Tatsächlich ist sein zweiter Name das murine Leukämievirus (MLV). In Zukunft wurde die Entwicklung auf sicherere Optionen umgestellt.
Was genau ist ein viraler Vektor? Dies ist ein speziell modifizierter Virus, der nur einmal funktioniert. Wie eine Spritze. Dazu muss er mehrere Kriterien erfüllen:
Sicherheit
Der virale Vektor sollte sich nicht spontan vermehren können. Dafür haben sie einen eingebauten Kill-Schalter. Ihr Genom ist zunächst so geschädigt, dass sie sich nicht autonom vermehren können. In einer Laborumgebung vermehren sie sich in der Zellkultur nur in Gegenwart unersetzlicher Komponenten und zusätzlicher Hilfsviren, die einen Teil der für die Assemblierung erforderlichen Proteine produzieren. Das heißt, es vermehrt sich in einem Laborkulturkolben, aber im Körper wirkt es einmal, verlässt die Zelle in halb zusammengesetzter Form und stirbt ab.
Geringe Zytotoxizität
Viele Viren sind sehr grausam gegenüber den Wirtszellen. Nach der Inkubationsphase stirbt die Zelle an Erschöpfung und neue Virionen streuen von ihren sterblichen Überresten in alle Richtungen. Gleichzeitig gibt es Viren, die die normale Physiologie der Zellen, auf denen sie parasitieren, nicht besonders beeinflussen. Zum Beispiel Adenoviren.
Stabilität
Viren müssen genetisch stabil sein. Zum Beispiel wird die Grippe nicht funktionieren. Er hat keine verständlichen Mechanismen der "Parität" und es ist ihm egal, dass der Hash nach dem Kopieren nicht konvergiert hat. Dies ist seine Evolutionsstrategie. Dieselben Coronaviren haben im Gegenteil Kontroll- und Reparaturmechanismen, die eine größere Stabilität des genetischen Materials bewirken. Obwohl sie aus anderen Gründen nicht als Vektor verwendet werden. Die Aufgabe besteht daher darin, sicherzustellen, dass das Virus bei seiner Reproduktion in Bioreaktoren dieselbe Nutzlast behält - die Nutzlast bleibt unverändert.
Zelltypspezifität
Der Virus muss seine Ladung nicht nur überall, sondern genau in einem bestimmten Zelltyp abgeben. Dies bedeutet, dass das Virus die multipotenten Vorläufer-Stammzellen von Blutzellen sehr genau infizieren muss, wenn wir eine mit defekten Erythrozyten verbundene Krankheit heilen müssen. Und haken Sie gleichzeitig nicht beispielsweise Muskelgewebe ein.
Was wird bereits in Bezug auf die Gentherapie getan?
Die erste humangenetische Korrektur wurde 1990 durchgeführt. Die 4-jährige Ashanti DeSilva wurde wegen eines schweren genetischen Defekts einer komplexen kombinierten Immunschwäche behandelt, der mit einem Mangel des ADA-Enzyms verbunden war. Es sollte beachtet werden, dass nicht das Genom von Stammzellen, die T-Lymphozyten produzieren, bearbeitet wurde, sondern adulte T-Zellen aus ihrem eigenen Spenderblut. Das heißt, sie musste diese Verfahren in Zukunft wiederholen. Dann gab es eine Reihe erfolgreicher experimenteller Protokolle zur Behandlung von SCID (schwerer kombinierter Immundefekt) unter Verwendung einer ähnlichen Technik.
1999 ereignete sich ein Vorfall, der die Forschung in diesem Bereich erheblich verlangsamte. Jesse Gelsinger litt an einer genetisch bedingten Lebererkrankung, aufgrund derer sie Ammoniak nicht entgiften konnte. 4 Tage nach der Einführung eines adenoviralen Vektors mit einer gesunden Kopie des Gens starb er an den Folgen einer Hyperimmunreaktion und eines Versagens mehrerer Organe. Anschließend kam die FDA zu dem Schluss, dass das Studienprotokoll zahlreiche Verstöße enthielt.
Im Jahr 2006 erschienen die ersten Berichte über erfolgreiche individuelle Gentherapieprotokolle zur Behandlung der Onkologie. Killer-T-Zellen werden für eine bestimmte Art von Tumor programmiert und dann in den Körper des Patienten freigesetzt. HIV-Therapie
im Jahr 2011 anerkanntbei Patient Gero Hütter im Jahr 2008. Die Methode ist nicht besonders für ein breites Publikum geeignet, da sie die vollständige Entfernung des Knochenmarks und die anschließende Implantation korrigierter Zellen mit einer doppelten Delta-32-Mutation erfordert, die den CCR5-Rezeptor deaktiviert.
Bis 2013 waren weltweit nur fünf Gen-Medikamente zugelassen. Drei aus der Onkologie, Glybera zur Behandlung von erblichem Lipoproteinlipasemangel und Neovaskulgen. Letzteres wurde übrigens komplett von uns entwickelt.
Neovasculgen
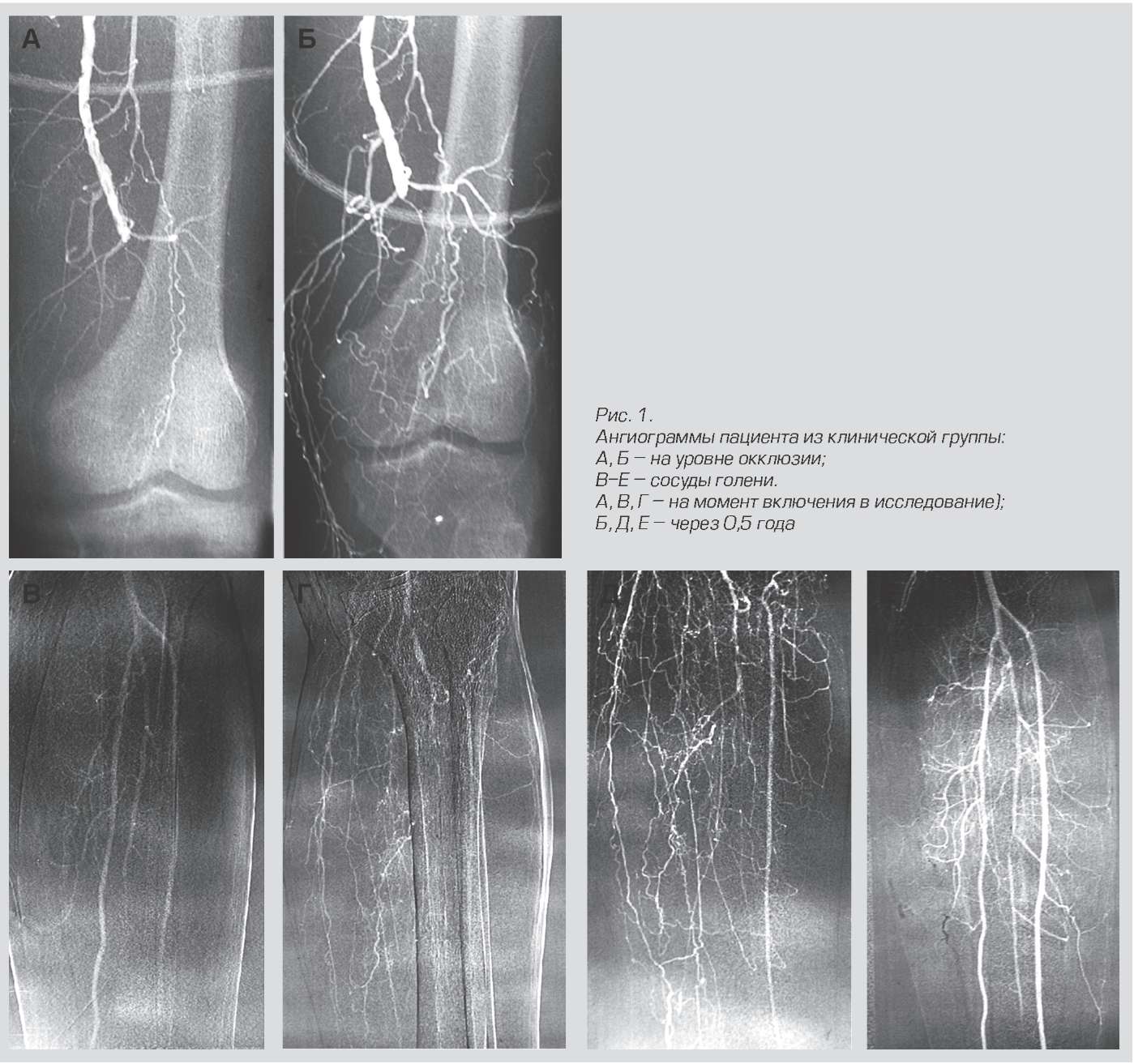
Ergebnisse der Behandlung mit Neovasculgen.
Dieses Medikament gehört zum Plasmid, dh es bearbeitet nicht sein eigenes Genom der Zelle, sondern liefert nur Plasmide, die für eine begrenzte Zeit wirken.
(), VEGF 165, (VEGF — Vascular Endothelial Growth Factor). , . , , .
Human Stem Cell Institute
Der Wirkungsmechanismus ist interessant. Die Zellen an der Injektionsstelle beginnen mit der Synthese von VEGF, einem vaskulären Wachstumsfaktor. Infolgedessen beginnt in diesem Bereich ein neues verzweigtes Kapillarnetzwerk zu wachsen. Dies ist beispielsweise bei Patienten mit chronischer Ischämie der unteren Extremitäten aufgrund von Diabetes und Atherosklerose von entscheidender Bedeutung. Vor diesem Medikament gab es weitere Amputationen. Jetzt wurde es auch für die Verwendung in der Zahnmedizin zur Implantation von Implantaten getestet. Das Genpräparat wird mit Knochenmaterial gemischt und genäht. Infolgedessen wachsen die Gefäße schnell und das notwendige Gewebe wird ohne Abstoßung gebildet. Die Kaninchen wurden bereits während der Transplantation von Schädelfragmenten genau simuliert. Soweit ich weiß, sind die Leute die nächsten.
Zolgensma
Die Muskelatrophie der Wirbelsäule ist eine sehr schlimme Erkrankung, die klinisch der Amyotrophen Lateralsklerose, an der Hawking litt, etwas ähnlich ist, aber andere Ursachen hat. Infolge der Entwicklung der Krankheit schreitet die Lähmung fort, die aufgrund der Unfähigkeit zu atmen zum Tod führt.
Zolgensma ist das erste gentherapeutische Medikament gegen spinale Muskelatrophie. Produziert von AveXis (Novartis). Eine Arbeitskopie des SMN-Gens wird unter Verwendung des Adeno-assoziierten Virus (AAV) Serotyp 9, AAV9, injiziert, der die Blut-Hirn-Schranke passieren und in die Zellen des Patienten gelangen kann. Ein Problem - es kostet absolut monströses Geld. Eine Injektion kostet mehr als 2,1 Millionen US-Dollar (etwa 152 Millionen Rubel). Aber die Ergebnisse sind auch erstaunlich. Beim Menschen wird die motorische Funktion wiederhergestellt und die Krankheit schreitet nicht weiter voran. Theoretisch sollten solche teuren Manipulationen vom Staat bezahlt werden. Für den Einzelnen sind die Kosten für die Behandlung seltener Krankheiten einfach unerschwinglich.
Was weiter?
Hier ist eine sehr schwierige Frage. Wir akkumulieren defekte Gene in der Bevölkerung. Früher starb ein Kind mit einem Herzfehler einfach - jetzt retten sie ihn und er gibt Nachkommen mit diesem Fehler. Früher dauerten viele Schwangerschaften nicht an - jetzt werden schwangere Frauen mit einem minimalen Prozentsatz an Fehlgeburten herausgezogen und mit erfolgreichen Geburten abgeschlossen. Tatsächlich brechen wir die Mechanismen der natürlichen Keulung der Bevölkerung. Dies ist richtig und menschlich, aber mit den akkumulierten Mutationen des Genpools muss etwas getan werden.
Entweder kommen wir zu Green Cards und Zuchtgenehmigungen, oder wir lernen, wie man genetische Anomalien zuverlässig und sicher korrigiert. Es wäre cool, Myopie, systemische Bindegewebsdysplasie und eine Reihe anderer Geburtsfehler zu beseitigen. Und schließlich das dumme kaputte Gen reparieren, das wie alle normalen Säugetiere für die Synthese von Vitamin C aus Glukose verantwortlich ist.
Hier erwartet uns nur eine unbekannte Zukunft weiter. Am alarmierendsten ist die mögliche Schichtung der Gesellschaft, wenn die reichsten Bevölkerungsgruppen ihre Kinder so verändern, dass sie frei von Diabetes und Arteriosklerose sind, und gleichzeitig ein wenig Myostatin zerdrücken, damit sie ohne große Anstrengung sportlich aussehen. Cool. Aber es macht Angst.
