Trainingsrelevanz
Ein wichtiges Stadium bei der Entwicklung der Klassifizierung der Ordnung der Flöhe ist mit der Entwicklung der genomolekularen Forschung verbunden. Gegenwärtig wird dank dieser Methoden die Verwandtschaft der Ordnungen von Flöhen und Mecopter bestätigt. Die Gene der ribosomalen DNA, der Elongationsfaktor der Proteinsynthese und das mitochondriale Gen Cytochromoxidase II (COII), die in Vertretern der meisten Familien der Mecopter-Ordnung untersucht wurden, sowie 128 Arten von 83 Gattungen von Flöhen aus 16 Familien werden aktiv untersucht (S.G. Medvedev. 2009; Whiting 2002; Whiting et al. 2008). Die Flohphylogenie wird auf der Grundlage von Daten zu diesen Genen durch verschiedene Methoden zur Konstruktion phylogenetischer Bäume und Modelle zur Berechnung paarweiser Abstände rekonstruiert, die häufig in Form eines Konsensbaums (Strick Consensus) dargestellt werden (Whiting et al. 2008). In einigen Fällen widersprechen die Ergebnisse genomolekularer Studien jedoch dem Schema familiärer Bindungen.auf der Grundlage einer phylogenetischen Analyse erhalten. Darüber hinaus kann in Übereinstimmung mit unterschiedlichen Interpretationen molekulargenetischer Daten der Ursprung der wichtigsten Infraorder von Flöhen auf unterschiedliche Weise interpretiert werden. Aus Sicht verschiedener Autoren können die gleichen Flohkladen sowohl polyphyletische als auch monophyletische Gruppen sein (Whiting et al. 2008, S. G. Medvedev. 2019). Dies kann sowohl auf die Besonderheiten der Ökologie der modernen Flohfauna als auch auf verschiedene methodische Probleme bei der Arbeit mit molekulargenetischen Daten zurückzuführen sein.und monophyletische Gruppen (Whiting et al. 2008, S. G. Medvedev. 2019). Dies kann sowohl mit den Besonderheiten der Ökologie der modernen Flohfauna als auch mit verschiedenen methodischen Problemen bei der Arbeit mit molekulargenetischen Daten zusammenhängen.und monophyletische Gruppen (Whiting et al. 2008, S. G. Medvedev. 2019). Dies kann sowohl mit den Besonderheiten der Ökologie der modernen Flohfauna als auch mit verschiedenen methodischen Problemen bei der Arbeit mit molekulargenetischen Daten zusammenhängen.
In Bezug auf den ersten Punkt sollte betont werden, dass die Isolierung getrennter phyletischer Flohlinien, die in der Taxonomie den gleichen Status haben, in verschiedenen historischen Intervallen erfolgte. Dies bedeutet wiederum, dass die Flohfauna verstreute Fragmente einer ausgedehnten Paläofauna sind, die inzwischen weitgehend ausgestorben ist (S.G. Medwedew. 2009, S.G. Medwedew. 2019). Daraus folgt, dass wir mit unterschiedlichen methodischen Ansätzen für genetische molekulare Studien die konvergente Entwicklung von Nukleotidsequenzen (Homoplasie) aus den Augen verlieren können, was zu Fehlern bei der Bestimmung der Topologie des Baumes und zu einer geringen statistischen Unterstützung von Zweigen führen kann. So können beispielsweise Daten verwendet werden, die unterschiedliche Beziehungen für unterschiedliche Taxa und dementsprechend unterschiedliche Beziehungen zu unterschiedlichen Regionen von Genen aufweisen.Wir werden Lücken in den Sequenzen und das Fehlen von Daten für verschiedene Loci für verschiedene Proben finden (S. G. Medvedev. 2019, Lukashov V. V. 2006). Daher sollten bei der Auswahl einer Forschungsmethode all diese Probleme berücksichtigt und Proben der am besten untersuchten und häufigsten Floh-Taxa ausgewählt werden, um sie dann mit den am meisten untersuchten Mecopter-Proben zu vergleichen. Auf diese Weise können wir einen zuverlässigeren Baum mit hoher Unterstützung erstellen.
, Siphonaptera Mecoptera -II (COII).
:
Siphonaptera NCBI [5], .
(COX 1) Siphonaptera .
-II (COII) Mecoptera Siphonaptera NCBI [1].
MEGA X.
.
NCBI [5] : Chaetopsylla globiceps (Taschenberg, 1880), Chaetopsylla trichosa (Kohaut, 1903), Ctenocephalides felis (Bouché, 1835), Ctenocephalides canis (Curtis, 1826), Ceratophyllus sciurorum (Schrank, 1803), Leptopsylla segnis (Schönherr, 1811). , NCBI[1], Boreus: Boreus westwoodi (Hagen, 1866), Boreus hymalis (Linnaeus, 1767), Boreus coloradensis (Byers, 1955), Boreus nivoriundus (Fitch, 1847), Boreus brumalis (Fitch, 1847), Boreus californicus (Packard, 1870), (.1.).
UPGMA [2] , - 500 [3]. Muscle (. 2.) MEGA X [4]. Muscle . , . translate DNA to protein and vice versa (.3), . (. 3.) , - , . (.4). MEGA . Modeltest 3.06 PPC (Posada, D., Crandall, K.C., 1999) (AIC), . AIC , , (Posada, D., Buckley, T.R., 2004.). MEGA X [4] 64- Windows 10 Home 4- INTEL 1,6 1 .
- [6] (.5.). 12 . 1-+2-+3-+. ( ). 742 .
( 1.)

(.2.)
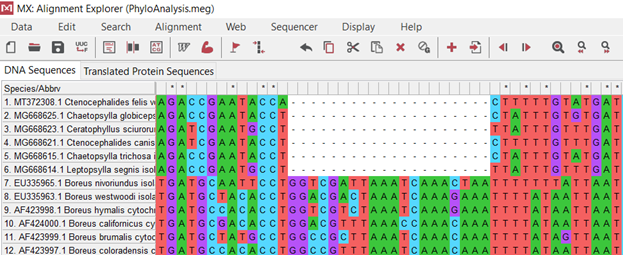
(.3.)
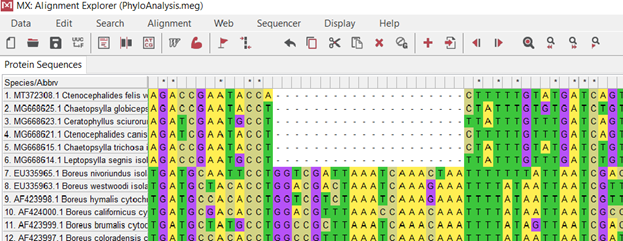
(.4.)
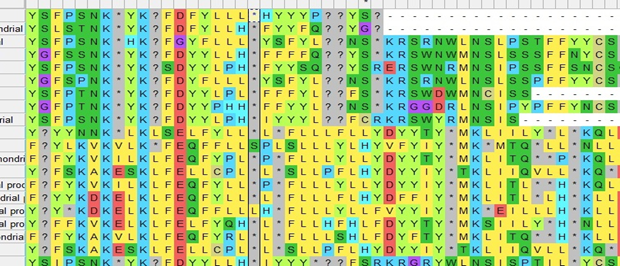
(.5)
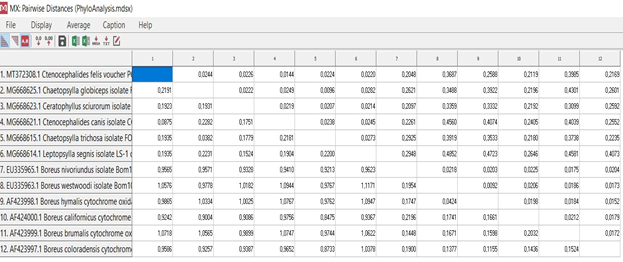
. Mecoptera Siphonaptera. 60% , Mecoptera Siphonaptera. , , , .
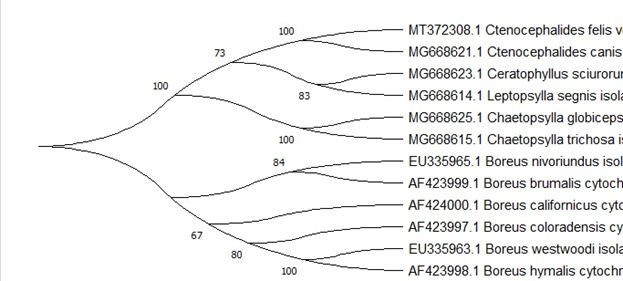
, MEGA X [4] (80%-100%) , . Ceratophyllus sciurorum Leptopsylla segnis (73%), . , (.. .2009; Whiting 2002; Whiting et al. 2008).
Mecoptera Siphonaptera . . Boreus nivoriundus Boreus brumalis (80%) «» Chaetopsylla globiceps Chaetopsylla trichosa (100%). , Mecoptera Siphonaptera. Boreus californicus (67%) . , . (.6.)
(.6.)
. . , , , . . . . [https://vk.com/phanerozoi] . , .
.
, , .
, .
1. Whiting M.F. 2002. Mecoptera is paraphyletic: multiple genes and phylogeny of Mecoptera and Siphonaptera. Zoologica Scripta, 31: 93–104
2. Whiting M.F., Whiting A.S., Hastriter M.W. and Dittmar K. 2008. A molecular phylogeny of fleas (Insecta: Siphonaptera) and host associations. Cladistics, 24: 1–31.
3. , .. , 313, № 3, 2009, c. 273–282
4. (SIPHONAPTERA) .., .. III , 2009, . 185-190
5. / .. —.. , 2009. — .256. .29-31.
6. Posada, D., Buckley, T.R., 2004. Model selection and model averaging in phylogenetics: advantages of the AIC and Bayesian approaches over likelihood ratio tests. Syst. Biol. 53, 793–808.
7. Posada, D., Crandall, K.C., 1999. Modeltest. Bioinformatics 14, 817–818.
1. http://lifemap.univ-lyon1.fr
2. Sneath P.H.A. and Sokal R.R. (1973). Numerical Taxonomy. Freeman, San Francisco.
3. Felsenstein J. (1985). Confidence limits on phylogenies: An approach using the bootstrap. Evolution 39:783-791
4. Kumar S., Stecher G., Li M., Knyaz C. und Tamura K. ( 2018 ). MEGA X: Molekulare evolutionäre Genetikanalyse über Computerplattformen hinweg. Molecular Biology and Evolution 35 : 1547 & ndash; 1549.
5.https: //www.ncbi.nlm.nih.gov/pmc/articles/PMC4681159/
6. Tajima F. und Nei M. ( 1984 ). Abschätzung des evolutionären Abstands zwischen Nukleotidsequenzen. Molecular Biology and Evolution 1 : 269 & ndash; 285.